평생 약을 먹어야 하는 병?
떨림, 근육 경직, 느려지는 동작. 파킨슨병 환자들이 겪는 이 증상들의 공통점이 무엇인지 아는가?
바로 뇌 속 도파민 생성 뉴런의 점진적 사멸이다. 도파민은 운동 조절에 필수적인 신경전달물질이며, 이것이 부족해지면 우리 몸의 움직임이 제대로 작동하지 않는다.
문제는 대부분의 파킨슨병 환자가 평생 약물치료를 받아야 하며, 장기 복용 시 심각한 부작용이 발생한다는 것이다. 레보도파(L-DOPA)는 파킨슨병의 핵심 치료제지만, 장기 사용 시 50% 이상의 환자에서 이상운동증(dyskinesia)을 유발한다(2019, Movement Disorders Journal). 도파민 작용제는 충동 조절 장애, 환각, 우울증 등 심각한 정신과적 부작용과 연관되어 있다.
그렇다면 약물 대신 세포 수준에서 뉴런을 보호할 수 있는 방법은 없을까?
미토콘드리아 손상을 발견하다
최근 신경과학계에서는 파킨슨병의 근본 원인으로 미토콘드리아 기능 장애를 주목하고 있다.

미토콘드리아는 세포의 발전소다. ATP(에너지)를 생성하는 핵심 기관이다. 나이가 들면서 산화스트레스가 미토콘드리아 DNA를 손상시키고, ATP 생산이 감소하며, 결국 도파민 뉴런이 죽게 된다.
이는 단순히 도파민이 부족한 것이 아니라, 왜 뉴런이 죽는가에 대한 답이다.
특히 주목할 점은, 파킨슨병 환자의 뇌에서 미토콘드리아 복합체 I의 활성이 30-40% 감소되어 있다는 여러 연구 결과다. 이는 에너지 생산 능력의 직접적인 저하를 의미하며, 신경세포가 생존하기 어려운 환경을 만든다.
파킨슨병은 도파민 부족만의 문제가 아니다
많은 사람들이 파킨슨병을 단순히 “도파민이 부족한 병”으로 생각한다. 하지만 일부만 맞고 일부는 틀리다.
파킨슨병은 결과적으로 도파민 부족 증상을 보이지만, 근본 원인은 에너지 대사의 붕괴다.
첫째, 미토콘드리아의 과도한 분열(fission)이 세포 에너지 고갈을 유발한다. 둘째, 미토콘드리아의 융합(fusion) 능력이 저하되면서 손상 회복 메커니즘이 작동하지 않는다.
단순히 도파민을 약으로 보충하는 것이 아니라, 뉴런 자체를 살려내는 것이 핵심이다. 증상을 관리하는 것과 원인을 해결하는 것은 다르다.
PBM(Photobiomodulation)이 미토콘드리아를 회복시키는 방식
PBM은 단순한 빛 조사가 아니다. 세포 수준에서 에너지 생산 시스템을 복구하는 치료법이다.
특히 PBM은 특정파장을 이용해 미토콘드리아 내 시토크롬-C 산화효소를 자극하여 ATP 생성을 증가시킨다. 이는 약물이 할 수 없는, 세포의 근본적 회복 과정이다.

융합-분열 균형의 재조정
미토콘드리아는 끊임없이 융합(fusion)과 분열(fission)을 반복한다. 이 균형이 무너지면 세포 건강이 무너진다.
융합 단백질 (MFN1, MFN2, OPA1): 미토콘드리아를 합쳐서 손상을 복구하고 에너지 효율을 높인다.
분열 단백질 (DRP1, FIS1, MFF): 미토콘드리아를 나누는 역할을 하지만, 과도하게 활성화되면 세포 에너지 고갈과 세포 사멸을 유발한다.
PBM은 DRP1과 FIS1 같은 분열 유도 인자를 감소시키고, MFN1과 OPA1 같은 융합 촉진 인자를 증가시킨다. 이를 통해 미토콘드리아가 더 건강하고 에너지 효율적인 상태로 이동하며, 신경퇴행으로 이어지는 기능 장애의 연쇄를 예방한다(Trajano et al., 2024).
| 단백질 | 역할 | PBM 이후 | 효과 |
| DRP1 | 과도한 미토콘드리아 분열 유발 (부정적) | 감소 | 단편화 억제 → 에너지 보존 및 뉴런 생존 지원 |
| FIS1 | DRP1을 통한 분열 지원 (부정적) | 감소 | 세포 스트레스 감소 |
| MFN1 | 외막 융합 촉진 (긍정적) | 증가 | 더 큰 미토콘드리아를 통한 에너지 효율 향상 |
| OPA1 | 내막 안정화, 융합 지원 (긍정적) | 증가 | 막전위 유지, ATP 합성 개선 |
또한 PBM은 적색광(660nm)과 근적외선(850nm, 940nm) 파장을 사용하여 두개골을 투과해 뇌 조직 깊숙이 도달한다. 이는 피부나 근육 치료와 달리, 신경세포에 직접 작용할 수 있다는 의미다.
파킨슨병을 악화시키는 주범들
연구에 따르면, 다음과 같은 요소들이 미토콘드리아 기능을 저하시키고 파킨슨병을 악화시킨다.
산화스트레스: 활성산소가 미토콘드리아 DNA를 직접 손상시켜 ATP 생산 능력을 떨어뜨린다.
만성 염증: 뇌 내 신경염증(neuroinflammation)이 지속되면 도파민 뉴런이 더 빨리 사멸한다.
환경 독소: 살충제, 중금속 등은 미토콘드리아 복합체 I을 억제하여 에너지 대사를 방해한다.
수면 부족: 깊은 수면 중에 뇌세포의 손상이 복구되는데, 만성적인 수면 부족은 신경 회복 능력을 떨어뜨린다.
장내미생물 불균형: 장-뇌 축(Gut-Brain Axis)을 통해 장내 염증이 뇌로 전달되며, 파킨슨병 환자의 80% 이상이 변비 등 소화기 증상을 먼저 경험한다.
운동 부족: 규칙적인 운동은 미토콘드리아 생합성을 촉진하는데, 움직임이 줄어들면 뇌세포의 에너지 생산 능력도 함께 떨어진다.
광생체조절치료는 이러한 요인들로 인해 손상된 미토콘드리아를 회복시키고, 신경세포의 생존 환경을 개선하는 데 도움을 줄 수 있다.
임상 연구: 걸음 속도가 빨라졌다
파킨슨병 환자에게 걸음 속도는 단순한 숫자가 아니다. 이동성, 독립성, 낙상 위험을 직접적으로 반영하는 지표다.
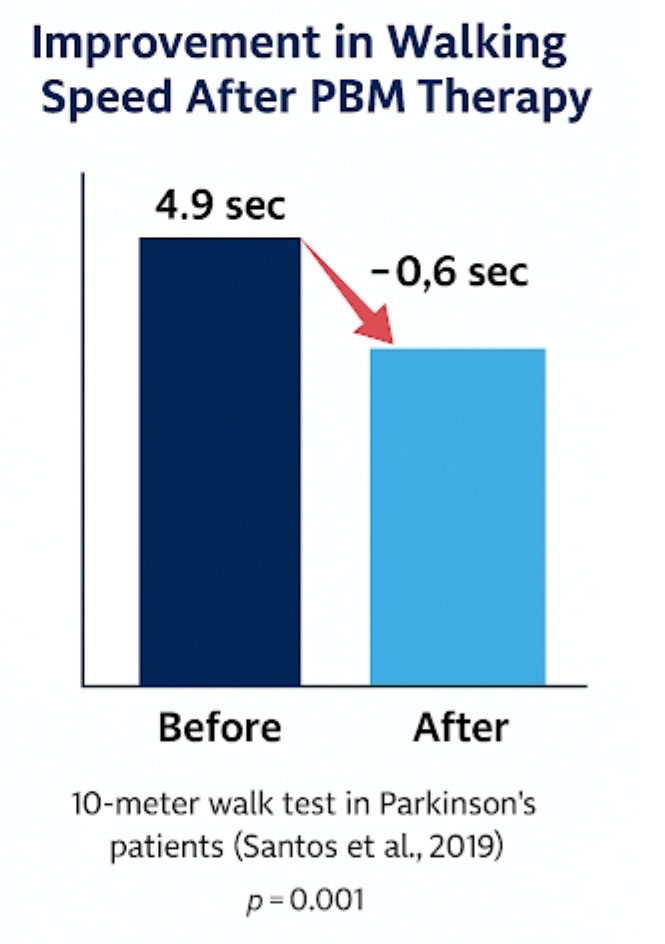
2019년 브라질 상파울루 대학교 Santos 연구팀이 Brain Stimulation 저널에 발표한 무작위 대조 연구(RCT)에서, 35명의 파킨슨병 환자가 9주간 광생체조절치료를 받았다. 10미터 보행 테스트에서 평균 걸음 속도가 0.6초 개선되었다(4.9초 → 4.3초, p=0.001).
이 결과는 임상적으로 의미 있는 최소 변화량(MCID, 0.23m/s)을 초과한다. 즉, 환자들이 일상생활에서 실제로 체감할 수 있는 수준의 기능 향상이다.
또한 이 연구에서 주목할 점은 부작용이 전혀 보고되지 않았다는 것이다. 약물 치료와 달리, PBM은 비침습적이며 신체에 해로운 영향을 주지 않는다.
치료의 미래는 세포에 있다
파킨슨병 치료를 단순히 ‘증상 억제’로만 접근하면 한계가 있다. 핵심은 뉴런을 살리는 것이다.
광생체조절치료는 도파민을 인위적으로 보충하는 대신, 도파민을 생성하는 뉴런 자체를 보호한다. 미토콘드리아 건강을 회복시키는 이 접근법은 임상 연구로 뒷받침되며, 알려진 부작용이 없다.
약물에만 의존하는 시대는 지나가고 있다. 세포 수준에서 뉴런을 보호하는 광생체조절치료는, 파킨슨병 환자들이 오랫동안 기다려온 돌파구가 될 수 있다.
당신의 뇌세포는 지금도 에너지를 필요로 한다. 미토콘드리아에 빛을 비춰라. 움직임이 돌아온다.